Chémia sily jednoduchých a skladacích anorganických rečí. Platnosť klasifikácie reči. anorganické reči
Anorganické reči - také chemické spoluky, ako v prípade organických ľudí, neberú z uhlia (okrem kyanidov, karbidov, karbonátov a niektorých tradičných).
Klasifikácia anorganických rečí je urážlivá. Existujú jednoduché slová: nekovy (H2, N2, O2), kovy (Na, Zn, Fe), jednoduché amfotérne slová (Mn, Zn, Al), vzácne plyny (Xe, He, Rn) a skladacie slová: oxidy (H20, CO2, P2O5); hydroxy (Ca (OH) 2, H2S04); soli (CuSO4, NaCl, KNO3, Ca3 (PO4) 2) a binárne spoluks.
Molekuly jednoduchých (jednoprvkových) slov sú uložené iba z atómov jedného (jedného) typu (prvku). Zápach sa neotvorí v drzých reakciách a nevyjde pred prijatím týchto prejavov. jednoduchá reč vlastným spôsobom môžu byť použité na kovové aj nekovové. Jasné hranice medzi nimi neukazujú duálnu moc prostredníctvom sily jednoduchých rečí. Deyaky prvky okamžite prejavujú silu a kov a nekov. Їx sa nazývajú amfotérne.
Noble gazi - tse anorganické reči blízko triedy; smrad virіznyayutsya pre-pre tých, ktorí majú špeciálnu kapacitu. VIIIA-skupina.
Stav vecí deyakyhských prvkov pozostáva z niekoľkých jednoduchých, ktoré sú vnímané ako budhizmus a moc, nazývané alotropia. Pre prvky C je možné použiť zadky, ktoré upevnia diamantovú karabínu a grafit; Pro - ozón a kisín; R - bilium, chervony, čierna a іnshі. Takýto jav je možné dosiahnuť zmenou počtu atómov v molekule a nastavením budovy s atómami rôznych kryštalických foriem.
Okrem jednoduchých základných tried neorganickej reči zahŕňajú skladacie spoluky. Skladacie (dvojsmerné, viacprvkové) reči sú vhodné na zber chemických prvkov. Molekuly Їх sú zložené z atómov nové druhy(Prvky Riznykh). Pri rozklade v chemických reakciách vytvorí zápach niekoľko slov. Zdieľajte na výstave a sol.
V minulosti boli atómy kovov oddelené od hydroxylových skupín (alebo jednej skupiny). Ideme k rastlinám (lúkam) a nie k vode.
Oxydis sú uložené v dvoch prvkoch, s jednou väzbou є kissen. Vôňa nie je soľotvorná a soľotvorná.
Hydroxidy sú reťazcom reakcií, ktoré sa vyvíjajú pri interakcii (priamej alebo nepriamej) s vodou. Označujú sa ako: podrobenie (Al (OH) 3, Ca (OH) 2), kyseliny (HCl, H2SO4, HNO3, H3PO4), (Al (OH) 3, Zn (OH) 2). Interakciou rôznych typov hydroxidov vzniká soľná kyselina.
Solitizujte v strede (skladujte z katiónu a aniónu - Ca3 (PO4) 2, Na2SO4); kyselina (na nahradenie atómov vodou v prebytku kyseliny, ktorú je možné nahradiť katiónmi -NaHSO3, CaHPO4), zásaditá (môže byť skladovaná v hydroxy -aboxo skupine -Cu2CO3 (OH) 2); sub (na nahradenie dvoch rôznych chemických katiónov) alebo / alebo komplexných (na nahradenie dvoch nadbytočných kyselín) solí (CaMg (CO3) 2, K3).
Binarni spoluky (aby dosiahli veľkú triedu reči) ísť po kyselinách a bez kyselín (H2S, HCl); soli bez kyselín (CaF2, NaCl) a ďalšie spoluky (CaC2, AlH3, CS2).
Anorganické reči neskrývajú uhlíkovú kostru, ktorá je základom organických spolucov.
V organizme ľudí є jak (34%), tak anorganické spoluks. Do zvyšku sa na prvé miesto dostáva voda (60%) a vápenaté soli, z ktorých sa tvorí kostra človeka.
Anorganickú reč v ľudskom tele predstavuje 22 chemických prvkov. Väčšina z nich je v kovoch. Už z koncentrácie prvkov v tele sa nazývajú mikro- (namiesto v tele nie viac ako 0,005% hmotnosti) a makroelementy. Nepostrádateľnými mikroelementmi pre telo sú jód, zalizo, med, zinok, mangán, molybdén, kobalt, chróm, selén, fluór. Nádej byť v organizme je potrebná pre normálny život človeka. Makroelementy ako vápnik, fosfor a chlór sú základom tkanín bagatokh.
Filozofická pravda: všetko v našej spoločnosti je prijateľné, - spravodlivé z hľadiska klasifikácie prejavov a autorít. Vo vesmíre na našej planéte dochádza k veľkým zmenám v reči, pričom všetky sú zbavené 90 chemických prvkov. V prírode sa objavujú reči, ktoré sú vyvolané prvkami so sériovými číslami od 1 do 91 vrátane. Prvok 43 je technický, v dánskej hodine nebol v prírode na Zemi odhalený, takže tento prvok nemá dostatok stabilných izotopov. Výsledkom je výhra buv otrimaniy po častiach jadrová reakcia... Hviezdy a názov prvku sú z vlašských orechov. téhnos - kus.
Všetky pozemské prírodné chemické reči, vychádzajúce z 90 prvkov, možno rozdeliť na dva veľké typy - anorganické a organické.
Organické frázy sa nazývajú spolucs v uhlí pre známku tých najjednoduchších: oxidy v uhlíku, karbidy kovov, oxidy kyselín a solí. Všetky prejavy sú uvedené ako anorganické.
Existuje 27 miliónov organických rečí - je ich viac, menej anorganických, počet tých pre najoptimistickejších pidrachunkov nie je 400 tisíc. Budeme hovoriť o dôvodoch zmeny organických spór, ale väčšinou nie je dôvod na rýchle oddelenie týchto dvoch skupín slov. Izokyanát amónny NH4NCO napríklad používajú neekologické výrobky a sekcia (NH2) 2CO, ktorá je presne tým istým elementárnym skladom N2H4CO, je organická.
Špecifikácie, ktoré môžu mať rovnaký molekulárny vzorec, aj keď chemický, sa nazývajú izoméry.
Anorganické reči sú prijaté rozdelením na dva podtypy - jednoduché a skladacie (schéma 1). Yak už vieš, oni to nazývajú jednoduché slová, ktoré sú zložené z atómov jedného veselý prvok, A skladanie - z dvoch alebo viacerých chemických prvkov.
Schéma 1
Klasifikácia anorganických rečí
Zdavalosya b, počet jednoduchých rečí je vinný počtom chemických prvkov. Nie je to však tak. Vpravo v skutočnosti, že atómy jedného a toho istého chemického prvku môžu vytvoriť nie jedno, ale niekoľko jednoduchých slov. Tento jav, ako viete, sa nazýva alotropia. Dôvodom alotropie môže byť počet atómov v molekule (napríklad alotropické modifikácie kyslého prvku - kyslíka a ozónu O3), ako aj rast kryštálovej mriežky pevnej reči (napríklad poznáme aj alotropia grafitu).
V type jednoduchej reči vidia kov, nekovy a vzácne plyny a ostatné sú často označované ako nekovy. Základom takejto klasifikácie je sila jednoduchých rečí, obohatenie atómov púčikov o chemické prvky, z ktorých sú reči stanovené, a typ kryštálovej mriežky. Všetky druhy vecí, mysleli si, že vedú elektrický brnk, vedenie tepla, plast, volodymy kovovú metlu. Nekovy sa spravidla s takýmito autoritami nevylučujú. Naša plachosť „spravidla“ nie je vipadkova, ale opäť platnosť klasifikácie jednoduchých slov. Deyak hodil nekovy za úrady (napríklad alotropická úprava cínu - sivý cín - prášok šedej farby, nevedie elektrický prúd, aby sa znížilo oslnenie a plasticita, to znamená ako žlčový cín, іnsha - alotropická úprava . Pre kov sú charakteristické Navpaki, nekovový grafit, alotropická modifikácia v uhlí, veľmi elektrické vodiče a volodya.
sám out-of-the-box klasifikácia skladanie anorganických rečí, dobrá znalosť chémie základnej školy. Tu vidíte triedu chotiri: oxidy, potraviny, kyseliny a soli.
Malo by sa to uskutočniť v triede pre neekologické prejavy v sklade, ktorá by v ich vlastnom dome mala byť zaslaná orgánom krajiny. Nagadaєmo označenie zástupcov triedy pokožky.
oxidy
- skladacia reč, ktorá je uložená v dvoch prvkoch, jedným z nich je kyselina v oxidačnom stupni -2 (napríklad H2O, CO2, CuO).
Pidstavi
- reťazec skladacích slov, ktorý je možné uložiť z atómu kovu a jednej alebo dvoch hydroxylových skupín (napríklad NaOH, Ca (OH) 2).
kyselina
- reťazec skladateľnej reči, ktorý je uložený z atómov vody a prebytku kyseliny (napríklad HCl, HNO3, H2SO4, H3PO4).
soľ
- veľa skladacej reči, ktorá je uložená z atómov kovu a prebytku kyseliny (napríklad NaNO3, K2SO4, AlCl3).
Podľa klasifikácie a doplnenia je možné tiež pridať. Úlohu kovu v potravinách a soli teda môžu hrať skladacie diely známych častí katiónu amónneho NH4 +, takže je možné skladovať iba nekovové prvky. Iným spôsobom je potrebné vykonať numerickú skupinu prejavov, ako sú formálne znaky (za skladom) є, na úrady a obrátiť sa na úrady o amfotérnych hydroxidoch, aby bolo možné konfrontovať úrady s dodávkou kyseliny. Napríklad hydroxid hlinitý Al (OH) 3 sa pri interakcii s kyselinou uskutočňuje nasledovne:
Al (OH) 3 + 3HCl = AlCl3 + 3H20,
a pri raftingu na lúkach sa prejavuje kyslá sila:
H3AlO3 + NaOH = NaAlO2 + H20.
Po tretie, klasifikácia skladacích anorganických rečí nie je konzumovaná v zameraných skvelé číslo z'udnan, pretože nie je možné ich priniesť do jednej z poistených tried. Napríklad z'udnannya zriadila dva alebo viac nekovových prvkov (chlorid fosforečný PCl5, sírovodík CS2, fosgén COCl2).
? 1. Hovoria sa reči anorganicky a čo sú organické? Vznášať zadok. Poskytnite platnosť takýchto klasifikácií rečí.
2. Aké slová sa nazývajú jednoduché a ktoré sú skladacie? Prečo počet jednoduchých slov mení počet chemických prvkov?
3. Yaka klasifikácia jednoduchých slov? Umiestnite zadky typu pokožky. Vzácne plyny є slová atómových alebo molekulárnych budov? Viesť argumenty do jadra týchto a іnshoi hľadísk.
4. Nazývajú sa anorganické slová oxidy, zásady, kyseliny, soli? Aby ste viedli slová triedy pokožky, ukážte silu dvoch alebo troch rovnakých chemické reakcie.
5. Kvôli ďalšej pomoci chemických reakcií upozornite, že amfotérne hydroxidy ukazujú silu kyselín aj zásad.
6. Uhličitan vápenatý (kreida, marmur, vapnyak) nadikhavskí sochári, výtvarníci, básnici. napríklad:
Téma: Reflexia odovzdaného materiálu
Lekcia: Klasifikácia anorganických rečí
V histórii vývoja chémie nové klasifikácie reč. Jeden z prvých znakov klasifikácie prejavov buv dzherelo їkh je odmietnutý. Pre veľkú znalosť reči pokračovali k roslinne (otriman z roslin), tvorom (otriman z tvarin) a minerálu (otriman z minineral).
J.Ya. Bercelius bol zjednotený v prejavoch, videných z roslínu a tvarínu, do skupiny organických a táto skupina sa nazývala anorganické reči. Existuje viac ako jedna klasifikácia slov: podľa kameniva, podľa farby, vône a podľa niektorých znakov.
Pre nás je dôležité systematizovať prejavy podľa ich charakteristík drzé úrady, Sklad Yaki viznachayutsya їkh. Celkovo je moderná klasifikácia anorganických rečí založená.
Jednou z prvých odrážok je klasifikácia rečových riadkov na jednoduché a skladanie stavaním pred skladaním. Akonáhle sa reč dostala do priestoru, bola presunutá do záhybu, pretože reč nešla do priestoru pre žiadnu myseľ - niekedy jednoduchú.
Postavili sa, takže budova bola pred distribúciou previazaná skladom reči. Jednoduché slová sú uložené z jedného chemického prvku a skladacie - z decilov.
Jednoduché slová sú spravidla rozdelené do dvoch tried: hodené a nekovové. Pre kovy, ako napr Fyzická sila, Yak kovová šľahačka, visoka tepelná a elektrická vodivosť, plasticita. Sila nekovov skončí v rozdiele, aj keď spravidla v páchnucom kriku a v špinavosti elektrikárov.
Malé. 1. Klasifikácia jednoduchých slov
Klasifikácia skladacej reči je viac skladacia. Voľbu triedy skladacej reči môžete vidieť v depozitoch zo skladu a silách: oxidy, potraviny, kyseliny a soli.
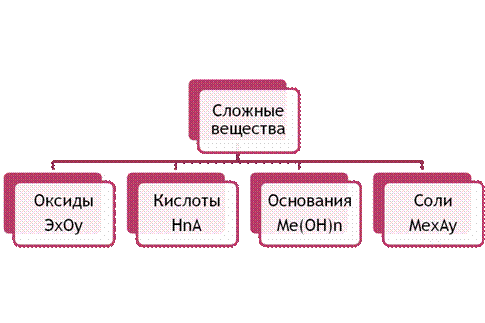
Malé. 2. Klasifikácia skladacej reči
Oxidy sa nazývajú binárne reči, pred ktorých skladisko vstupujú bozkávané. Počiatočný vzorec oxidov možno napísať nasledovne: E x O y. Kovy sa používajú na výrobu zásaditých oxidov a nekovy sú kyslé.
Mimochodom, nazývame skladacie slová, ktoré sú uložené v kovových a jednej alebo dokonca v decilových hydroxylových skupinách. Počiatočný vzorec je p_dstav Me (OH) n. Je nevyhnutné chodiť po lúke (mimo vody) a nie mimo kontroly v blízkosti vody.
Kyseliny sa nazývajú skladacie slová, ktoré sa ukladajú z atómov vo vode, budovy sú nahradené kovom a prebytok kyselín. Їx počiatočný vzorec možno zapísať v nasledujúcej hodnosti - H n A, de A - prebytok kyseliny.
Kyselina, pre jeden znak klasifikácie - prejav v sklade molekúl atómov, je kyslá - prechádza do kyslej a bez kyslej. Kisnevmіsnі kyseliny a podrobenie zlúčiť do skupiny slov pod názvom hydroxy.
Soli sa nazývajú skladacie slová, ktoré sa ukladajú na prebytok kovov a kyselín. Počiatočný vzorec je Me x A y.
Ale klasifikácia anorganických rečí nie je ani zďaleka dokonalá. Do akej triedy by napríklad mali byť údaje zaradené do chemického vzorca NH3 (amiak)? Oxid je tiež suchý, pretože nie je možné ho preniesť do kyslého ani zásaditého stavu. Napríklad N20, NO, CO sa nazývajú netvoriace soli (oxidy baiduzhimy).
1. Zbirnik zabdan a právo z chémie: 8. ročník: Navchan. P.A. Orzhekovsky i іn. „Khimiya. 8 trieda “/ P.A. Orzhekovskiy, N.A. Titov, F.F. Hegel. - M .: AST: Astrel, 2006. (s. 117-123)
2. Ushakova O.V. Pracujúci človek zaseje z chémie: 8. ročník: pred asistentom P.A. Orzhekovsky i іn. „Khimiya. 8 trieda “/ O.V. Ushakova, P.I. Bespalov, P.A. Orzhekovskiy; vyd. prof. P.A. Orzhekovsky - M .: AST: Astrel: Profizdat, 2006. (s. 120-123)
3. Chémia. 8 trieda. Učebnica pre zahraničné vzdelávanie. ustanovka / P.A. Orzhekovskiy, L.M. Meshcheryakova, M.M. Šalašova. - M.: Astrel, 2013. (§36)
4. Chémia: 8. ročník: Učebnica pre zahraničné vzdelávanie. ustanovka / P.A. Orzhekovskiy, L.M. Meshcheryakova, L.S. Pontak. M .: AST: Astrel, 2005. (§42)
5. Encyklopédia pre deti. Zväzok 17. Khimia / Ed. V.A. Volodin, viedol. vedecký. vyd. І. Leenson. - M.: Avanta +, 2003.
Dodatkovi webové zdroje
2. Chemické informácie o leme ().
Domov zavdannya
1.c. 122-123 č. 2,3 4 z Pracovná zoshita z chémie: 8. ročník: pred asistentom P.A. Orzhekovsky i іn. „Khimiya. 8 trieda “/ O.V. Ushakova, P.I. Bespalov, P.A. Orzhekovskiy; vyd. prof. P.A. Orzhekovsky - M.: AST: Astrel: Profizdat, 2006.
2. s.201 č. 1,3 od asistenta P.A. Orzhekovsky, L.M. Meshcheryakova, M.M. Shalashova „Khimiya: 8kl.“, 2013 s